Présentation du programme
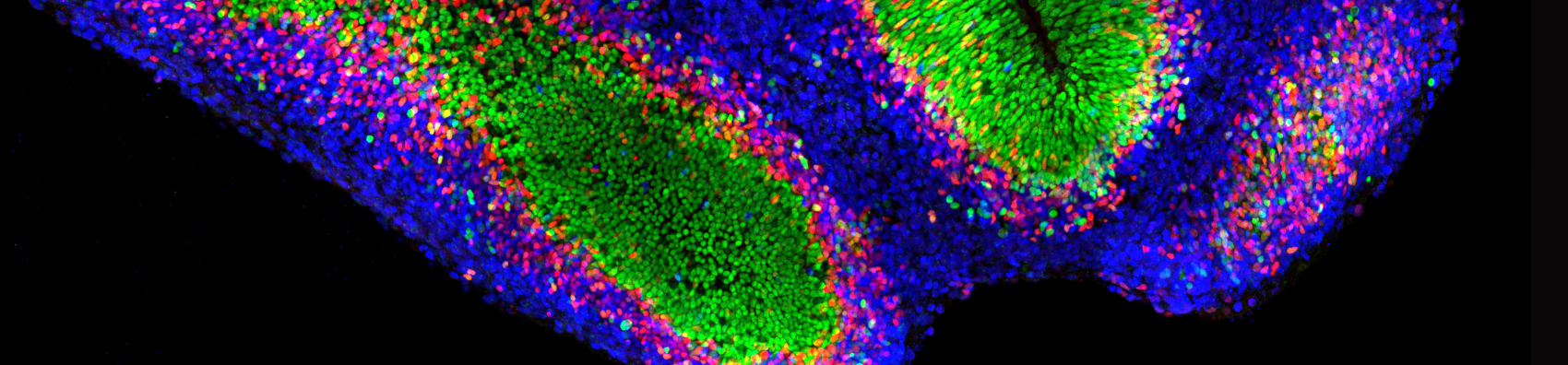
Identités et destins cellulaires

Un enjeu de santé publique majeur
En France, les tumeurs pédiatriques cérébrales sont les cancers les plus fréquents après les leucémies chez les enfants de moins de 15 ans. Elles touchent près de 500 nouveaux enfants chaque année (Chiffres 2021). La plupart des patients qui survivent subissent des traitements sévères et présentent des séquelles à long terme qui affectent leur qualité de vie et leur place dans la société. La prise en charge de ces maladies représente donc une charge individuelle, familiale et sociétale importante.
De manière plus générale, les tumeurs présentent une prolifération incontrôlée des cellules. Différents types de cancers sont à considérer selon les dérégulations cellulaires, les types de cellules concernées et le moment au cours de la vie auquel ces dérégulations se manifestent.
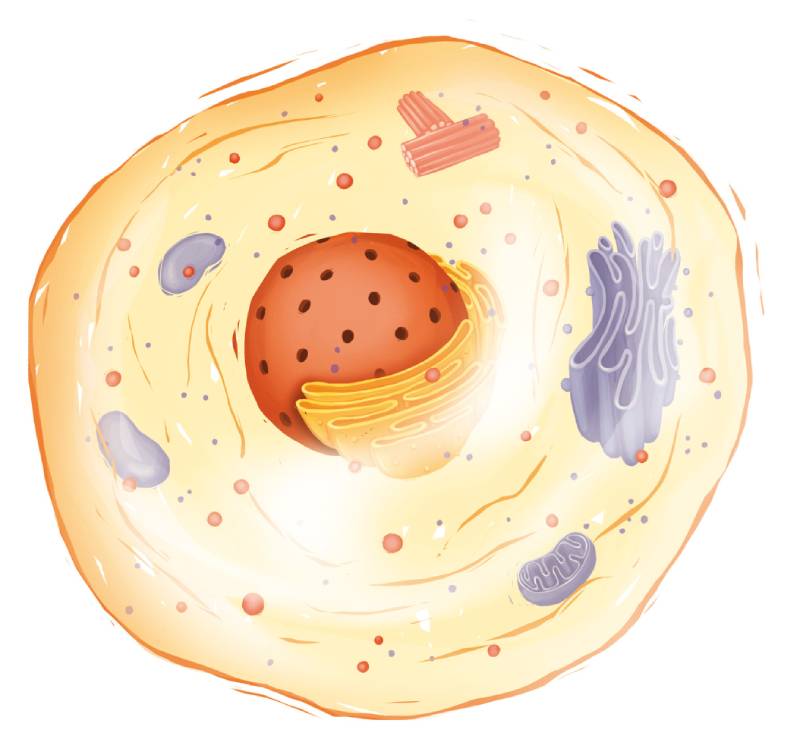
Qu’est-ce qu’une cellule ?
Une seule cellule, le zygote (ou œuf), résulte de la fécondation de l’ovocyte par le sperme et permet le développement d’un organisme entier. Elle permet en se divisant de produire l’ensemble des cellules qui constituent le corps humain, soit plus de 30 000 milliards de cellules distinctes ! Ces cellules différentes dans leur rôle partagent pourtant la même information génétique dans leur ADN. Chaque être humain possède un ADN, organisé en 23 paires de chromosomes qui permet de coder des milliers de gènes.
Des trajectoires qui déraillent
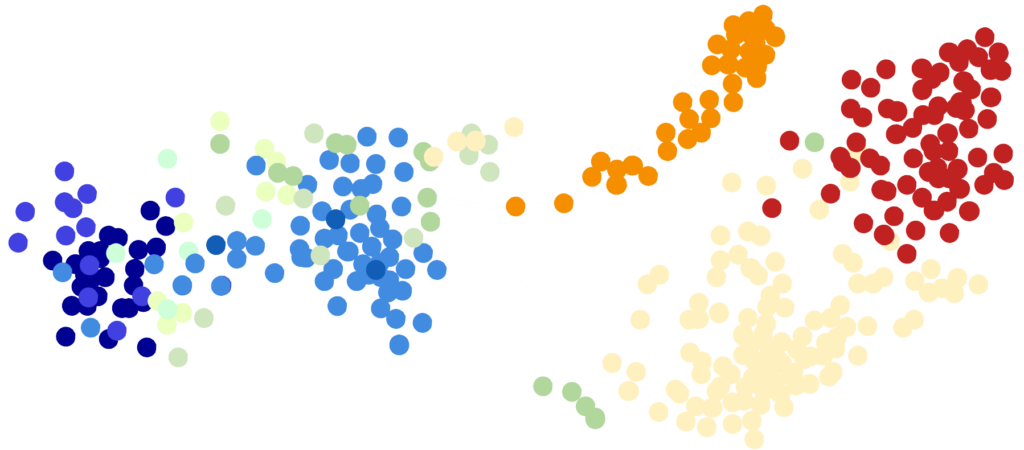
Au cours du développement d’un individu, cette information génétique peut être lue différemment afin de produire divers types cellulaires comme les neurones ou les cellules musculaires. Ainsi, des trajectoires ou destins cellulaires sont adoptées en utilisant différentes combinaisons de gènes. Ces trajectoires décrivent comment une cellule se spécialise et assure un rôle spécifique dans l’organisme. Cependant, cette lecture de l’information génétique peut être perturbée. Dans ce cas, la cellule peut suivre une trajectoire anormale à un mauvais moment. Ce type d’erreur peut à terme se manifester par des pathologies diverses, telles que des maladies inflammatoires, neurodégénératives, mais aussi différents types de cancer.
Le programme Cell-ID explore des questions cruciales en biologie du développement, plus particulièrement ciblées sur le développement neurologique et des cancers cérébraux pédiatriques résultants d’erreurs dans le programme de développement :
- Comment les cellules acquièrent-elles leur identité ? Chaque cellule possède un génome qui fonctionne de manière dynamique, il s’agit alors de comprendre comment sont générées les trajectoires cellulaires au cours du temps.
- Comment ces diverses populations cellulaires contribuent-elles à l’organisation en trois dimensions des tissus cérébraux ? Comment chaque cellule interagit dans le temps et l’espace avec ses voisines et son environnement est en enjeu important pour la formation d’un tissu sain. Cette construction avec les populations distinctes nécessaires pour le développement neurologique est à caractériser.
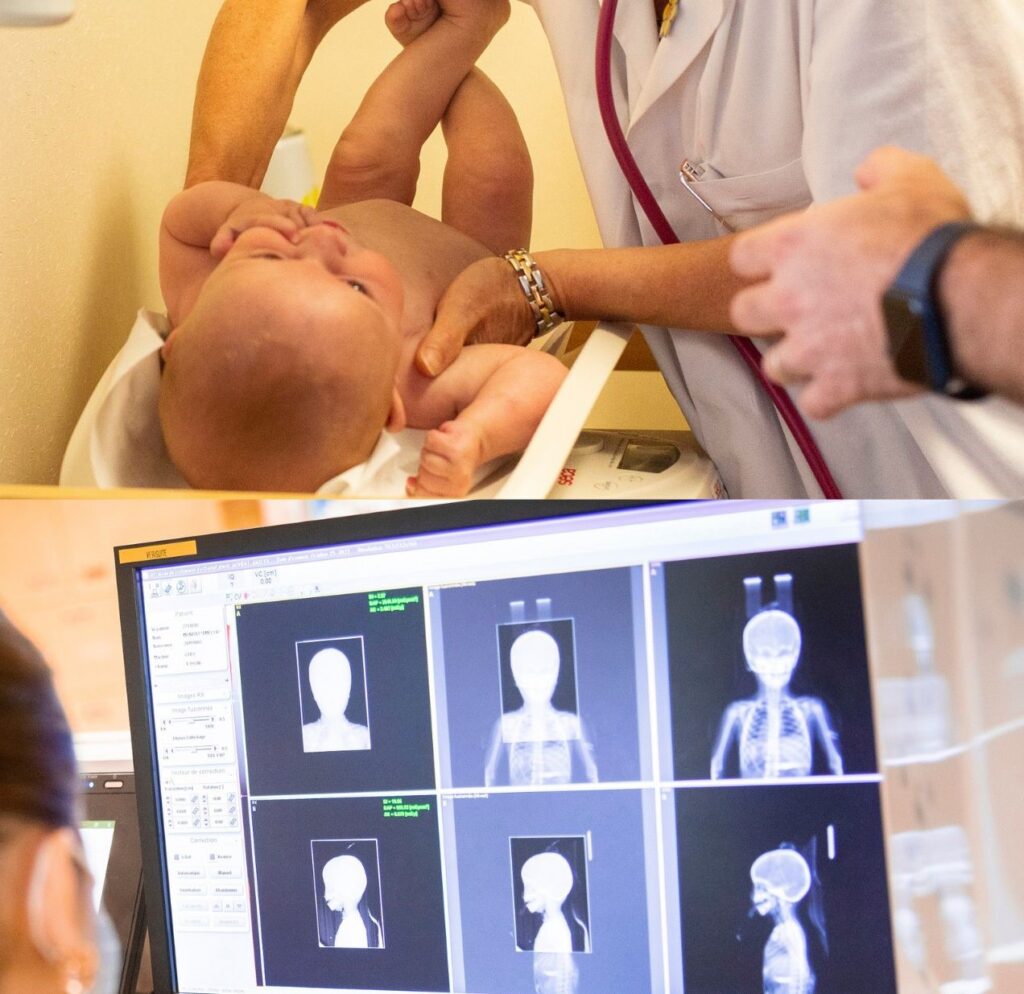
- Quelles sont les déviations non physiologiques impliquées dans l’apparition et la progression des tumeurs cérébrales chez l’enfant ? Actuellement, les enfants atteints de tumeurs cérébrales sont souvent diagnostiqués à un stade avancé, lorsque les cellules tumorales se sont déjà largement propagées dans le système nerveux central. Des progrès sont nécessaires pour disposer de méthodes de diagnostic plus précoces, non invasives, et détecter la maladie avant l’apparition de symptômes handicapants, ainsi que pour surveiller les patients à risque et prévenir les rechutes.
Trois obstacles principaux à surmonter
- L’expertise nécessaire pour mettre en œuvre ces technologies nouvelles, en les combinant entre elles, nécessite une recherche multidisciplinaire et un cadre spécifique pour la coopération et la coordination entre différents instituts de recherche et des ensembles hospitaliers.
- Les technologies à mettre en œuvre afin d’obtenir une résolution cellulaire, spatiale, et en fonction du temps dans des tissus complexes sont seulement en cours de développement.
- Le coût de ces nouvelles technologies reste élevé et demande des infrastructures spécialisées.


La mission de Cell-ID
Le programme de recherche Cell-ID « Identités et destins cellulaires » vise à comprendre les mécanismes qui régissent les identités et les destins cellulaires, et à déterminer quand et comment les cellules déraillent. Pour cela, il s’agit d’étudier le développement physiologique du système nerveux, et en parallèle, certains cancers pédiatriques du cerveau, dont l’origine serait due à une dérégulation du destin cellulaire durant le développement embryonnaire.
Les approches
Il s’agit d’utiliser des méthodes d’imagerie et de génomique fonctionnelle en partie basées sur les technologies de séquençage dites de « nouvelle génération » à très haut débit, combinées à l’analyse et la modélisation de ces données. Il faut également disposer de systèmes mimant les propriétés de tissus complexes normaux ou pathologiques. Ces combinaisons d’approches et d’outils sont des atouts importants pour comprendre quand et comment une cellule suit un destin particulier en conditions physiologiques pour établir un référentiel. La même stratégie peut alors se décliner pour comprendre comment la cellule perd son identité et dérive par rapport à son destin initial lors de pathologies.
Les résultats attendus
Cell-ID, en s’appuyant sur l’initiative LifeTime 2020 et le concept de médecine d’interception cellulaire, a le potentiel de faire avancer la compréhension des mécanismes cellulaires sous-jacents au développement neurologique, de promouvoir des avancées technologiques et favoriser la formation de la prochaine génération de scientifiques interdisciplinaires. À terme, cette initiative ouvrira la voie à l’amélioration du diagnostic, à l’évaluation du risque de progression ou de récidive de la maladie et à l’adaptation des traitements aussi précocement que possible. Le cas des cancers pédiatriques du cerveau représente un premier exemple de pathologie, mais les mêmes approches pourraient s’appliquer à d’autres pathologies à l’avenir.
Quatre axes synergiques
- Le projet ciblé (PC1) nommé CELL CONTEXT vise à identifier les stratégies optimales combinant des technologies émergentes, tout en développant de nouvelles technologies pour analyser dans le temps et dans le tissu cellulaire comment le génome fonctionne à l’échelle de chaque cellule.
- Un deuxième projet ciblé (PC2) nommé CELL EXP est dédié au développement d’approches sur des systèmes modèles pour l’étude de l’interaction entre cellules et le suivi spatio-temporel de leur destin. Les chercheurs utiliseront notamment des organoïdes régionalisés – structures multi-cellulaires 3D cultivées in vitro, imitant des régions spécifiques d’organes ou de tissus capables de simuler des pathologies – ainsi que des méthodes de visualisation de données. Ces organoïdes permettront d’intervenir avec des outils moléculaires sur les trajectoires cellulaires durant le développement embryonnaire du système nerveux.
- Un troisième projet ciblé (PC3) nommé DATA MED intègre deux volets, impliquant d’une part le développement de modèles prédictifs de trajectoires cellulaires à partir de données biologiques déjà disponibles. Ce premier volet sera essentiel en comparaison au second se focalisant sur les données qui seront produites sur des modèles expérimentaux et des données dérivées de tumeurs. Des premières hypothèses sur les déviations de trajectoire des cellules pour les tumeurs étudiées pourront être dégagées et testés expérimentalement sur les modèles de tumeurs les plus pertinents.
- Un quatrième projet ciblé (PC4) CELL NEXT a pour objectif de mettre en œuvre un programme de formation original et de développement de carrière conçu sur-mesure. Il servira de ciment pour les collaborations entre laboratoires et les projets innovants engageant la communauté Cell-ID.
Les actions clés
- Le recrutement de doctorants et post-doctorants ;
- Des actions de formation et d’animation à travers des colloques multidisciplinaires et des écoles d’été ;
- Des actions de communication vers la communauté scientifique et le grand public ;
- Des interactions avec les associations de patients
- Le montage de projet avec un effet levier ;
- Des projets innovants avec preuves de concept.
Les découvertes issues de ce programme permettront des avancées majeures pour les technologies, les méthodes et leur application au cerveau et les pathologies sélectionnées. Au-delà de ces pathologies, les progrès réalisés pourraient également permettre d’envisager des applications à d’autres maladies. Ce projet est donc une opportunité unique pour structurer la communauté scientifique française et la placer à la pointe de la recherche internationale dans ce domaine prometteur de la médecine cellulaire d’interception.
